L’immuno-hématologie est une branche de la médecine qui étudie les interactions entre les composants du système immunitaire et ceux du sang, surtout pour assurer la compatibilité lors des transfusions sanguines et la gestion des maladies hématologiques.
L’immuno-hématologie permet aux infirmier(e)s de comprendre les enjeux de la transfusion sanguine.
Cet article abordera la composition du sang et mettra l’accent sur des éléments tels que le plasma, les globules rouges, les globules blancs, les plaquettes et leur rôle dans la transfusion.
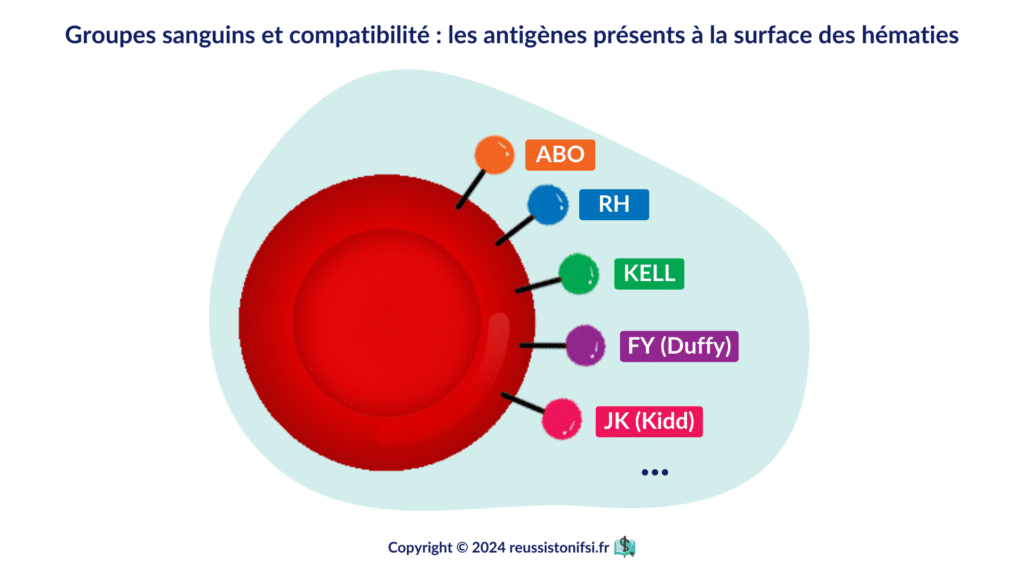
L’importance des groupes sanguins et de leur compatibilité sera également étudiée, en particulier les systèmes ABO et Rhésus et les règles de compatibilité, ainsi que d’autres antigènes de surface des globules rouges qui influencent la compatibilité transfusionnelle.
Comprendre les composants du sang
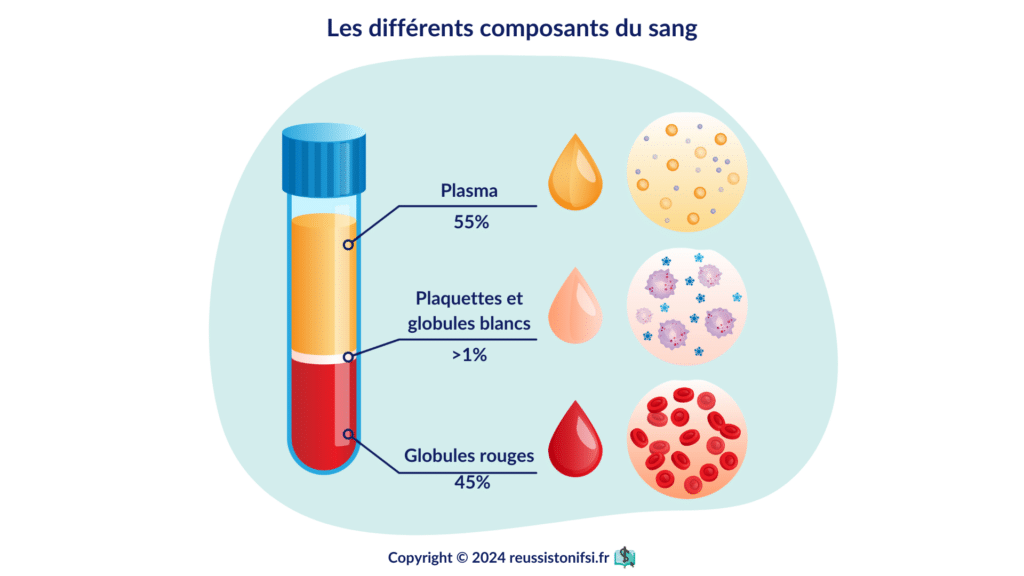
Le sang est composé de plasma et d’éléments figurés.1
La volémie, ou masse sanguine totale, varie selon des facteurs tels que le sexe, le poids, l’âge et l’altitude à laquelle une personne vit, son état d’hydratation, ses maladies chroniques, etc. En moyenne, elle représente 7 à 8 % du poids corporel d’un adulte, soit environ 5 à 6 litres.
Le plasma
Le plasma, qui est la composante liquide du sang, représente environ 55 % de sa composition totale. Il transporte des nutriments, des hormones et des protéines dans l’organisme. Il sert aussi de moyen d’évacuation des déchets métaboliques.
Le plasma transporte également des protéines spécialisées appelées anticorps, ou immunoglobulines, qui sont des éléments du système immunitaire. Produits par les plasmocytes, des cellules dérivées des lymphocytes B, les anticorps ont la capacité unique de reconnaître des structures spécifiques appelées antigènes. Les antigènes, souvent situés à la surface des cellules, y compris les agents pathogènes, sont comme des « drapeaux » qui caractérisent la cellule. Si l’antigène fait partie des antigènes appartenant à l’organisme, celui-ci ne se défendra pas contre lui-même et ne fabriquera pas d’anticorps. Si l’antigène est inconnu de l’organisme, il sera détecté par son système immunitaire, qui lancera une réponse immune pour le neutraliser et l’éliminer. La production d’anticorps, capables de se lier à l’antigène, est l’un de ces mécanismes de défense immunitaire.
En transfusion sanguine, cette interaction entre antigènes et anticorps est fondamentale, car une incompatibilité peut entraîner des réactions graves. C’est pourquoi la détermination précise du groupe sanguin et la compatibilité entre donneur et receveur sont fondamentales pour garantir la sécurité de la transfusion.
La compatibilité se décline selon trois règles : 2
1) Ne pas transfuser un PSL porteur d’un antigène pour lequel le receveur a, ou a eu, un anticorps.
Une telle transfusion crée un conflit immunologique immédiat (la fixation des anticorps du receveur sur les cellules transfusées) qui va neutraliser ou détruire le PSL, ce qui pourra être mortel s’il s’agit de globules rouges et rendra la transfusion inefficace s’il s’agit de plaquettes.
Si le malade a été immunisé contre cet antigène, mais n’a plus d’anticorps au moment de la transfusion, il s’ensuivra une restimulation de la production d’anticorps et un conflit immunologique retardé de quelques jours.
2) Éviter de transfuser un PSL comportant des anticorps qui vont reconnaître un antigène présent sur les cellules du receveur.
Les anticorps transfusés vont reconnaître et détruire les cellules du malade. Selon la quantité d’anticorps transfusés, donc selon la quantité de plasma contenue dans le PSL, l’impact pour le malade sera important ou pas.
3) Éviter de transfuser un PSL porteur d’un antigène que le receveur ne possède pas.
La présentation d’antigènes “étrangers” au système immunitaire du malade pourra déclencher une immunisation, avec la production d’anticorps.
En règle générale, ces anticorps n’apparaîtront en masse qu’une fois que le PSL transfusé aura disparu chez le malade et il n’y aura pas de conflit immunologique. En revanche, ces anticorps seront une barrière immunologique supplémentaire pour les prochaines transfusions.
Les éléments figurés du sang
Les éléments figurés, qui constituent les 45 % restants, comprennent trois types de cellules essentielles pour nos fonctions vitales :
- Les globules rouges (érythrocytes) : principaux transporteurs d’oxygène grâce à la protéine hémoglobine, ils donnent au sang sa couleur caractéristique et apportent l’oxygène des poumons aux différentes parties du corps et ramènent le dioxyde de carbone aux poumons pour son expulsion.
- Les globules blancs (leucocytes) : acteurs de notre système immunitaire, ils nous protègent contre les infections et les maladies. Ils sont capables de reconnaître et de neutraliser les agents pathogènes, comme les bactéries, les parasites et les virus.
- Les plaquettes (thrombocytes) : essentielles à la coagulation sanguine, elles réagissent en cas de lésion vasculaire en formant un caillot pour prévenir les saignements excessifs.
Groupes sanguins et compatibilité : les systèmes ABO, RH et les autres
Le système ABO
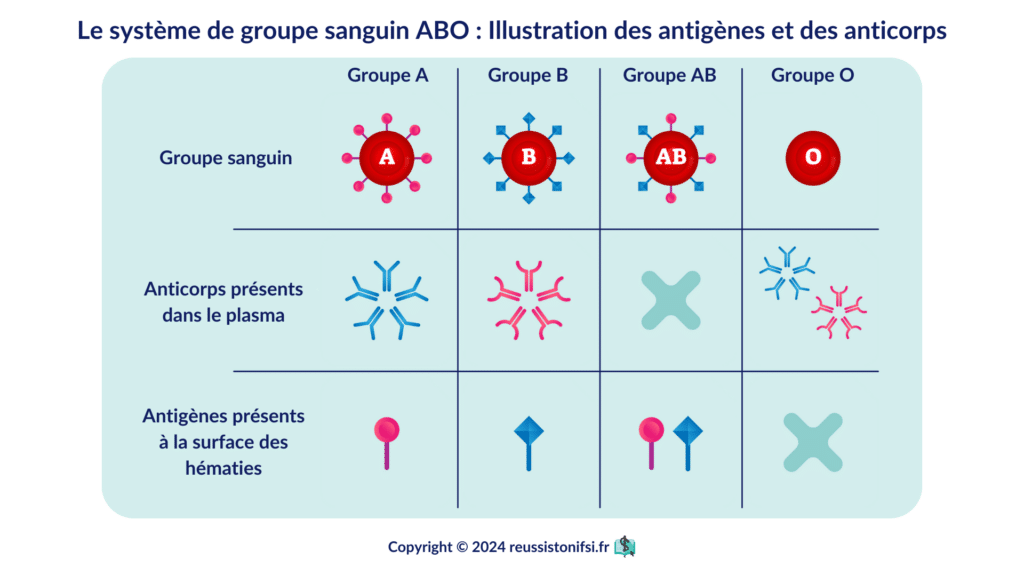
Les systèmes ABO et Rh représentent des marqueurs génétiques héréditaires, tout comme la couleur des yeux ou des cheveux, définis par la présence d’antigènes spécifiques à la surface des globules rouges. Comme les clés d’un puzzle biochimique, ces antigènes déterminent l’appartenance à l’un des quatre grands groupes sanguins : A, B, AB et O.
- Le groupe A possède uniquement l’antigène A sur les globules rouges.
- Le groupe B est caractérisé par la présence de l’antigène B.
- Le groupe AB contient à la fois les antigènes A et B. Le groupe AB peut recevoir des globules rouges de n’importe quel autre groupe, d’où son surnom de « receveur universel ».
- Le groupe O, dépourvu d’antigènes A et B, peut donner des globules rouges à n’importe quel autre groupe, ce qui lui vaut le titre de « donneur universel ».
En situation d’urgence, quand le groupe ABO du malade n’est pas connu, le sang O est TOUJOURS utilisé, car il est compatible avec tous les autres.3.4
L’importance de ces groupes sanguins lors d’une transfusion de CGR est critique.
Tout individu est systématiquement porteur des anticorps contre les antigènes ABO qu’il ne possède pas :
- Les malades de groupe A ont tous des anticorps anti-B.
- Les malades de groupe B ont tous des anticorps anti-A.
- Les malades de groupe AB n’ont pas d’anticorps anti-A ou anti-B.
- Les malades de groupe O ont tous des anticorps anti-A et anti-B.
Ces anticorps anti-A ou anti-B sont qualifiés de réguliers (et parfois de naturels).
Si les globules rouges transfusés ne sont pas compatibles, les anticorps présents dans le plasma du receveur peuvent attaquer les antigènes des hématies du donneur, et ainsi provoquer une agglutination et une destruction des globules rouges. Ce phénomène, appelé hémolyse, peut entraîner des complications sérieuses. D’où l’importance de tester la compatibilité sanguine avant toute transfusion.1
Attention, pour la transfusion de plasma, les compatibilités sont inversées, car le plasma contient des anticorps du donneur.

Le système Rhésus
Le système Rhésus (RH), souvent noté simplement par un + ou un -, indique la présence (RhD+) ou l’absence (RhD-) de l’antigène D sur les globules rouges. La combinaison des systèmes ABO et Rhésus conduit à huit groupes sanguins principaux : A+, A-, B+, B-, AB+, AB-, O+, et O-.1.4
Un individu avec des hématies RhD+ peut recevoir des globules rouges RhD+ et RhD-, mais les individus avec des globules rouges RhD- doivent généralement recevoir du sang RhD- pour éviter une immunisation anti-D.
Contrairement au système ABO, tous les autres systèmes de groupes sanguins ne contiennent pas systématiquement d’anticorps. Il faut qu’il y ait eu une première rencontre avec l’antigène étranger pour que le malade s’immunise et produise des anticorps dits « irréguliers ».2
Le système RH est un système complexe, qui va bien au-delà de l’antigène RHD. Dans le contexte transfusionnel courant, 4 autres antigènes sont déterminés dès lors qu’un individu est groupé :
- L’antigène C.
- L’antigène E.
- L’antigène c.
- L’antigène e.
La règle est la même que celle décrite ci-dessus pour l’antigène D. Les patients avec un antigène positif peuvent recevoir des globules rouges avec ou sans cet antigène, mais les malades négatifs pour cet antigène doivent généralement recevoir des globules rouges négatifs pour éviter une immunisation contre cet antigène.
Le système KEL
Un troisième système de groupe sanguin, le système KEL, est pris en compte dans la transfusion courante, pour un seul de ses antigènes, dénommé K, qui est positif ou négatif. La règle ci-dessus s’applique aussi pour lui.4.5
Analyses de laboratoire
Du point de vue des analyses de laboratoire, tous les antigènes que nous venons de voir sont systématiquement déterminés à l’occasion du bilan pré-transfusionnel d’un receveur, ainsi qu’à l’occasion du don. Ceci fusionne deux anciennes analyses qui étaient jadis dissociées :
- Le groupage sanguin : groupe ABO et RHD.
- Le phénotypage RH-KEL : le reste du RH (C, E, c, e) et l’antigène K.
Les résultats sont également exprimés en nomenclature internationale, qui permet de contourner l’ambiguïté potentielle de cette écriture en lettres (les antigènes RH D, C, E, c, e sont respectivement les antigènes RH1, RH2, RH3, RH4 et RH5; l’antigène KEL K est dénommé KEL1).
Système Kidd / Duffy / MNS
Dans le maquis considérable des groupes sanguins érythrocytaires (plus de 300 antigènes répartis sur plus de 30 systèmes de groupes sanguins), en dehors des systèmes ABO, RH et KEL qui sont utilisés au quotidien, trois autres systèmes présentent un intérêt transfusionnel fréquent chez certains malades : 6
- Le système Kidd ou JK.
- Le système Duffy ou FY.
- Le système MNS.
Ils seront déterminés chez les malades dans certaines situations. La règle qui leur est alors appliquée est la même que ci-dessus. Du point de vue des examens de laboratoire, on parlera de phénotypage complémentaire.
Qu’est-ce que la recherche d’anticorps anti-érythrocytaires irréguliers (RAI) ?
La RAI, ou recherche d’agglutinines irrégulières, est un test sanguin effectué pour détecter des anticorps irréguliers dans le sang d’une personne. Ces anticorps peuvent réagir contre certains types de globules rouges transfusés et doivent être identifiés avant une transfusion sanguine. Ce test aide à s’assurer que le sang transfusé est compatible avec celui du patient en plus de la carte de groupe sanguin, pour éviter l’apparition de complications.
Cette procédure implique la réaction du sérum du patient avec des échantillons d’hématies de groupe O dont les phénotypes sont déjà connus.
La RAI peut donner un résultat négatif ou positif.
RAI positif
Lorsque le test RAI est positif, le sérum du patient contient des anticorps irréguliers qui réagissent contre certains antigènes présents sur les globules rouges.
Ce résultat oblige à poursuivre l’analyse avec une étape d’identification des anticorps détectés, réalisée par le même laboratoire s’il en a le savoir-faire, ou par un autre laboratoire dans le cas contraire. Attention : dans ce dernier cas, si le laboratoire initial ne se charge pas de transférer le tube au second laboratoire, un nouveau prélèvement devra être réalisé et adressé au second laboratoire (consulter la procédure interne de l’établissement).
Les patients avec une RAI positive changent définitivement de statut transfusionnel, même si cette RAI se négative par la suite. Il leur est attribué deux protocoles : “phénotypé” et “compatibilisé”.
- Le protocole “phénotypé” implique que tous les globules rouges qui seront transfusés devront impérativement être compatibles avec les systèmes RH et KEL, c’est-à-dire ne jamais apporter d’antigène pour lequel le malade serait “négatif”. Il impose également l’absence de tout autre antigène pour lequel le malade aurait un anticorps irrégulier. Selon le cas, il peut aussi impliquer le respect des antigènes négatifs du malade pour les systèmes JK, FY et MNS.
- Le protocole “compatibilisé” implique que les concentrés de globules rouges choisis pour le malade devront, avant d’être délivrés pour transfusion, être testés au laboratoire avec le sang du malade, pour s’assurer de l’absence de tout conflit immunologique. Ce protocole, qui décale le moment de la transfusion, peut être annulé en situation d’urgence.
RAI négatif
Un résultat négatif indique que le sérum du patient ne contient pas d’anticorps irréguliers détectables. Le sang compatible avec le groupe ABO et Rhésus du patient peut être utilisé pour la transfusion.
Généralement, la RAI reste valide pendant trois jours, mais cette période peut être étendue à vingt et un jours dans certaines situations, comme en l’absence d’antécédents transfusionnels ou d’autres épisodes immunisants (tels que grossesse ou greffe) au cours des six mois précédents, sur décision médicale spécifique ou dans le cadre d’un protocole transfusionnel prédéfini.
De plus, la RAI est également pratiquée après la transfusion, dans l’idéal entre un et trois mois plus tard4, pour détecter l’émergence de nouveaux anticorps, car leur concentration plasmatique peut diminuer et devenir indétectable avec le temps.
Tout malade ayant été transfusé doit quitter l’établissement avec une ordonnance pour réaliser cette RAI post-transfusionnelle dans le laboratoire de son choix.
Cette analyse est également une composante du suivi prénatal des femmes enceintes, réalisée selon des directives spécifiques pour prévenir les complications liées à l’incompatibilité des groupes sanguins entre la mère et le fœtus.2
Connaissance et maîtrise des composants sanguins : un enjeu clé en transfusion
La connaissance approfondie des composants du sang, des groupes sanguins et de leur compatibilité, ainsi que des processus tels que la recherche d’anticorps anti-érythrocytaires irréguliers (RAI) garantissent la sécurité et l’efficacité des transfusions sanguines.
Nous espérons que ce guide vous aidera à mieux connaître les différents composants sanguins afin de sécuriser votre pratique infirmière. Si vous souhaitez davantage d’informations sur l’acte transfusionnel, nous avons rédigé un Guide infirmier : la transfusion.
Remerciements :
Nous tenons à exprimer notre profonde gratitude au Dr Jean-Yves PY (Société Francophone de Transfusion Sanguine) pour sa relecture attentive de cet article et sa précieuse contribution.
Chez Réussis ton IFSI, nous nous engageons à proposer des contenus d’une fiabilité inégalée. En complément de l’expertise interne de notre équipe habituelle, nous valorisons l’apport de professionnels extérieurs qualifiés qui enrichissent nos articles de perspectives nouvelles.
Sources
- Réussis ton IFSI « UE 2.2 – Le sang » 11/2023
- Conférence Nationale des Coordonnateurs Régionaux d’Hémovigilance et de sécurité transfusionnelle (CNCRH) « Les groupes sanguins » 10/03/2009
- University of Texas Southwestern Medical Center – Manuels MSD « Présentation de la transfusion sanguine » Ravindra Sarode – Mis à jour en 02/2022
- Société Francophone de Transfusion Sanguine (SFTS) « Diaporama pour l’enseignement de la transfusion sanguine dans les IFSI » 02/05/2019
- Ministère de la Santé et des Solidarités « Instruction N° DGS/PP4/DGOS/PF2/2021/230 du 16 novembre 2021 relative à la réalisation de l’acte transfusionnel » 16/11/2021
- Fasquel, C. (2019). La transfusion sanguine pour l’infirmier : Évaluation de l’UE 4.4 S4 – Stages – Pratique professionnelle